来源:医学术
重!磅!消!息!
据5月28日消息,注射用甲苯磺酸瑞马唑仑(瑞倍宁®)结肠镜III期数据已被American Journal of Translational Research(IF=3.266)接收。

此前其Ia、Ib期注册研究已于2020年2月被Clinical Therapeutics(IF=2.935)接收,其II期胃镜、II期全麻、III期胃镜和III期肠镜研究结果于1月份被欧洲麻醉学会选为2020年年会的壁报并做口头报告。
中国智造不断在国际舞台唱响!

甲苯磺酸瑞马唑仑Ⅲ期研究结果
注射用甲苯磺酸瑞马唑仑用于结肠镜诊疗镇静有效性和安全性研究是一项随机、单盲、阳性药物平行对照的全国多,Ⅲ期临床试验。
该研究纳入了384名接受结肠镜检查的患者,并将其随机分为甲苯磺酸瑞马唑仑和丙泊酚两组,在给予基础镇痛药芬太尼后分别给予甲苯磺酸瑞马唑仑和丙泊酚进行麻醉。
甲苯磺酸瑞马唑仑组,给予5mg初始剂量,后续追加剂量为2.5mg/次。丙泊酚组初始剂量为1.5mg/kg,追加剂量为0.5mg/kg/次。
结果显示,甲苯磺酸瑞马唑仑组镇静成功率96.91%(188/194)非劣于丙泊酚组100.00%(190/190)。
此外与丙泊酚组相比,甲苯磺酸瑞马唑仑组镇静低血压的发生率(23.71% vs 51.05%, P<0.0001)以及呼吸抑制的发生率(3.09% vs 16.84%, P<0.05)更低,不良事件和不良反应的发生率也更低,两组都没有出现严重的不良事件。

*甲苯磺酸瑞马唑仑结肠镜III期临床试验技术路线
甲苯磺酸瑞马唑仑的前世今生
前世――瑞马唑仑的研发历程

*瑞马唑仑开发历程
瑞马唑仑是一种短效苯二氮䓬类GABAA受体激动剂。葛兰素史克(GSK)公司在90年代后期发现了瑞马唑仑这一游离碱,并在2000年提交专利,随后授权CeNeS公司研发。

*瑞马唑仑与瑞芬太尼侧链结构相同
谈及瑞马唑仑的研发之路,不得不提到瑞芬太尼这一个起效迅速,主要通过血浆酯酶代谢的阿片类镇痛药。
瑞马唑仑的开发受到瑞芬太尼的启发,摒弃此前仅从咪达唑仑主环修饰苯二氮䓬类药物的传统观念,从软药角度出发,在苯二氮䓬母环上引入可以代谢的丙酸甲酯侧链。因此瑞马唑仑与瑞芬太尼的代谢途径类似,主要经血浆酯酶水解代谢,在体内不蓄积,代谢产物无活性,从而具有起效、失效迅速,镇静恢复时间短的特点。
由于瑞马唑仑游离分子只能在低温5℃的条件下保存,后由PAION公司改进并开发出更加稳定的苯磺酸瑞马唑仑,目前该药物在全球多个国家由多家企业研发,但目前均未获批上市。
今生――甲苯磺酸瑞马唑仑(瑞倍宁®)的研发历程
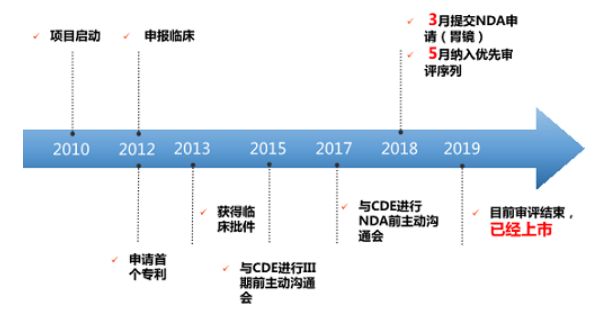
*甲苯磺酸瑞马唑仑研发历程
2010年,恒瑞医药启动甲苯磺酸瑞马唑仑新药研发项目。
2012年7月,距离启动仅两年时间,恒瑞医药研发出甲苯磺酸瑞马唑仑,所选甲苯磺酸成盐后具有更高的光学纯度和更佳的安全性,也因此获得了该盐型的专利,并经基础试验后开始申报临床试验;
2013年4月,获得中国化药1.1类临床批件。
2018年4月,经CFDA纳入优先审评,入选理由为“与现有治疗手段相比具有明显治疗优势”。
2019年12月27日,注射用甲苯磺酸瑞马唑仑(瑞倍宁®)正式上市。
出世――甲苯磺酸瑞马唑仑(瑞倍宁®)的获批之路
目前甲苯磺酸瑞马唑仑在国内共开发三大适应症:胃镜、结肠镜诊疗和择期手术全麻。
2012年恒瑞医药研发出甲苯磺酸瑞马唑仑后随即开始临床前基础研究,并于2013年开始临床试验。
2019年12月获批上市,同时被列入第二类精神药品管理,首批适应症为胃镜诊疗;结肠镜诊疗适应症申请已被CDE纳入优先审批通道,预计2021年获批。
全麻适应症已经完成了II期、III期临床试验,目前处于III期数据处理中,预计2022年获批。
未 来 可 期
未来恒瑞医药还将陆续开展甲苯磺酸瑞马唑仑在ICU镇静、支气管镜镇静等领域的临床研究,为临床用药提供更多循证医学证据,产生新的高光时刻!